税光厚研究组揭示神经酰胺合成酶2在调控肝脏病理多倍性的机制中取得新的进展
发布时间:2022.01.30
鞘脂作为细胞膜的主要结构成分之一,在信号转导和膜运输中发挥着重要的控制因子作用。神经酰胺是所有鞘脂类物质的主干,由长链鞘氨醇通过酰胺键与不同链长的脂肪酸结合而成。神经酰胺合成酶(CerS1-CerS6)有六种亚型,每种亚型具有合成不同酰基链长的神经酰胺(C14:0-C30:0)的能力,并具有组织特异性分布。神经酰胺合成酶2 (Ceramide synthase 2, CerS2)是CerS家族中表达最广泛的基因,具有“管家基因”之称。在小鼠肝脏(肝细胞)和肾脏组织中尤其高表达。CerS2优先合成酰基链较长的C22:0、C24:0和C24:1的神经酰胺。针对特异性合成较长N-酰基链长神经酰胺的CerS2开展科学研究,对进一步探究特定酰基链长的鞘脂的生理功能具有非常重要意义。
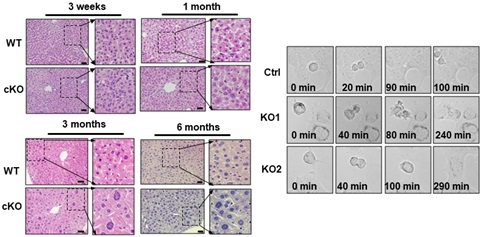
中国科学院遗传与发育生物学研究所税光厚研究组通过组织形态学和流式细胞术等实验方法发现CerS2敲除小鼠肝脏细胞出现异常的染色体多倍性和肝癌表型。利用S期特异性标记基因PCNA和有丝分裂期PHH3对小鼠肝脏组织进行免疫荧光染色,表明CerS2敲除后肝细胞障碍在M期。为此,研究人员利用活细胞成像技术做了深入分析,表明CerS2敲除后肝细胞发生不完全胞质分裂。通过脂质组学和蛋白组学进行深入分析,脂质组学数据显示CerS2敲除的肝脏组织中特定链长的鞘脂和磷脂则发生紊乱。蛋白组学分析发现有丝分裂阻滞缺陷蛋白2 (Mitotic arrest deficient 2, Mad2)表达量显著升高。Mad2表达量升高引起下游有丝分裂驱动蛋白样蛋白2功能缺陷进而导致肝细胞不完全胞质分裂出现异常染色体倍性的表型。同时,体外构建了CerS2基因敲除细胞系,通过活细胞成像,免疫染色,敲降Mad2等一系列实验手段进一步明确CerS2缺失是通过mad2介导的通路诱导细胞分裂缺陷进而引起肝脏病理多倍性的表型。本研究初步揭示了CerS2在维持肝脏染色体稳态和监测肝脏功能方面发挥着重要的作用,为进一步研究特定链长的鞘脂在肝癌中的作用性提供了新的科学思路。
该成果于2022年1月29日在线发表在《Clinical and Translational Medicine》上(https://doi.org/10.1002/ctm2.712),遗传发育所税光厚研究组已毕业博士生曹明君为本文的第一作者,税光厚研究员为该文章的通讯作者。该研究得到了科技部重点研发计划和国家自然科学基金委项目资助。